陈宇航研究组合作揭示小麦Sr35抗病小体的分子机制研究
| 来源:遗传所【字号:大 中 小】
农作物病虫害是制约农业生产的重要因素,严重威胁我国粮食安全。抗病蛋白作为最大的植物免疫受体家族可感知病原菌的存在,迅速启动免疫应答和抗病过程,是粮食稳产高产的重要保障。抗病蛋白如何激发免疫和抗病的分子机制研究一直植物领域的重大科学问题。此前,周俭民/陈宇航/何康敏/柴继杰研究组的合作研究揭示拟南芥ZAR1抗病小体形成可通透钙离子的离子通道,通过钙信号来激发植物免疫应答(DOI:10.1016/j.cell.2021.05.003)。然而,抗病小体在不同植物是否具有保守的共性机制尚不清楚。
清华大学/德国科隆大学柴继杰研究组、德国马普所Paul Schulze-Lefert研究组和中国科学院遗传与发育生物学研究所陈宇航研究组通过结构生物学,植物遗传学和电生理学等多学科交叉合作,阐明了小麦Sr35抗病小体的结构和分子机制。该研究首次揭示小麦抗病受体蛋白Sr35可被小麦杆锈病病原菌的效应因子AvrSr35所识别而激活,并进一步寡聚化形成抗病小体。合作研究团队利用冷冻电镜技术解析了Sr35抗病小体的五聚化结构,结合细胞生物学和电生理学等手段进一步阐明了Sr35抗病受体蛋白配体识别及活化的分子机制。
这些研究表明该Sr35抗病小体与之前研究的ZAR1抗病小体在三维结构和离子通道活性具有保守的共性机制,通过形成钙离子通道来激发免疫和抗病过程。该工作为CNL类抗病蛋白的跨物种改造及利用奠定了理论基础。该项研究成果在农业生产上具有广泛应用前景。合作研究团队还基于结构研究对感病作物的非功能同源蛋白进行精准改造获得抗病功能,为抗病农作物精准设计提供新思路。该研究成果于2022年9月26日以题为“A wheat resistosome defines common principles of immune receptor channels”在Nature杂志发表(DOI:10.1038/s41586-022-05231-w)。
柴继杰组Alexander Forderer、Ertong Li、Paul Schulze-Lefert研究组Aaron W. Lawson和陈宇航组博士生邓亚楠(2022毕业)为论文的共同第一作者,柴继杰教授、Paul Schulze-Lefert教授和陈宇航研究员为论文的共同通讯作者。该研究得到中国科学院战略先导专项和科技部等基金资助。
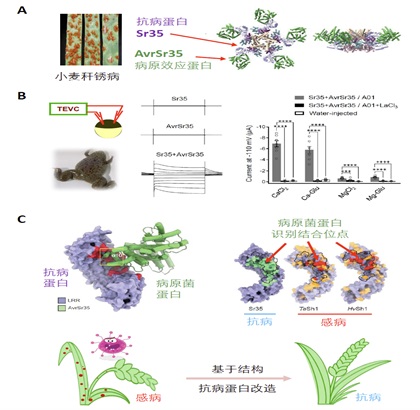
小麦抗病小体Sr35离子通道的分子机制研究
A. 小麦抗病蛋白Sr35识别小秆锈病病原菌效应蛋白AvrSr35,
激活形成Sr35抗病小体;
B. 通过非洲爪蟾卵母细胞的双电极电压钳电生理学研究
揭示Sr35抗病小体可形成通透钙离子的离子通道,
进而激发免疫和抗病过程。C. 基于结构研究的抗病农作物精准设计。
